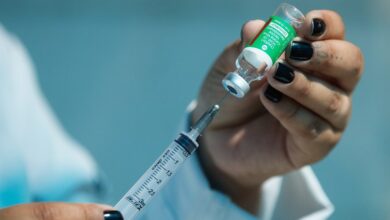
Anvisa autoriza retomada de testes da vacina CoronaVac

A Anvisa (Agência Nacional de Vigilância Sanitária) anunciou, nesta quarta-feira, 11, que os testes da CoronaVac, a vacina desenvolvida pelo laboratório chinês Sinovac para a Covid-19, serão retomados no Brasil.
“A Anvisa informa que acaba de autorizar a retomada do estudo clínico relacionado à vacina CoronaVac, que tem como patrocinador o Instituto Butantan”, disse a agência, em nota.
Segundo a Anvisa, a causa do evento adverso que levou à suspensão dos testes está em investigação. O boletim de ocorrência relacionado à causa foi enviado para a agência, pelo Instituto Butantan, às 23h43 de terça-feira, 10, de acordo com o comunicado desta quarta.
“A Anvisa entende que tem subsídios suficientes para permitir a retomada da vacinação e segue acompanhando a investigação do desfecho do caso para que seja definida a possível relação de causalidade entre o EAG [evento adverso grave] inesperado e a vacina”, diz a nota.
O texto diz, ainda, que a Anvisa “não está divulgando a natureza” do evento adverso ocorrido “em respeito à privacidade e integridade dos voluntários de pesquisa”.
Retomada – Ao suspender os testes, a Agência havia decidido que eles não seriam retomados até que os dados sobre o evento adverso fossem enviados pelo Comitê Internacional de Segurança. Isso ocorreu, segundo o órgão, na tarde de terça-feira, 10.
Os testes haviam sido suspensos pela agência na noite de segunda-feira, 9. Na ocasião, a Anvisa disse, sem dar detalhes, que um “evento adverso grave” havia ocorrido.
Embate – A suspensão levou a um embate entre a Agência e o Instituto Butantan, em São Paulo, que tem uma parceria com a Sinovac para fabricar a vacina e conduzir os ensaios de fase 3 no Brasil. Logo após o anúncio da pausa, o diretor do instituto, Dimas Covas, disse estranhar a decisão da agência, porque o evento adverso se tratava de um “óbito não relacionado à vacina”.
Na terça-feira, 10, um boletim de ocorrência obtido pela TV Globo indicou que a morte do voluntário foi um suicídio.
Pouco depois, em coletiva de imprensa, o diretor da Anvisa, Antonio Barra Torres, disse que “objetivamente, não havia essa informação [sobre a causa da morte] entre as que recebemos ontem [segunda-feira]”. Ele afirmou que a suspensão dos testes da CoronaVac foi “técnica” e baseada na falta de informações.
O Butantan, por outro lado, afirmou ter enviado duas vezes cópias das notificações à Anvisa sobre a morte do voluntário. O instituto disse que as informações sobre o caso foram enviadas pela primeira vez na sexta-feira, 6, e reenviadas no começo da noite de segunda-feira, 9, horas antes de a suspensão do estudo ser comunicada à imprensa.
O diretor da Anvisa, Antonio Barra Torres, disse, ainda na coletiva, que a suspensão seria mantida até que todas as informações sobre a morte de um voluntário fossem apresentadas junto com a análise do caso por um comitê internacional.
Mais tarde, ainda na terça-feira, 10, a Agência informou que havia recebido os dados dos testes enviados pelo comitê. Essa era a última atualização do caso até esta quarta-feira, 11.
Fonte: G1